2020年4月16日,中国食品药品检定研究院(以下简称:“中检院”)第八期注册检验用体外诊断试剂国家标准品和参考品目录正式发布了肿瘤突变负荷检测国家参考品(编号:360042),菁良基因很荣幸成为其协作单位之一。

肿瘤突变负荷,英文全称Tumor MutationBurden(TMB),是一种可定量的生物标志物,用来反映肿瘤细胞中所含有的突变数目,通常用肿瘤细胞基因组编码区的每百万碱基突变数来衡量。
TMB计算最早基于全外显子测序技术(WES),但是WES价格高昂,具有较多的临床应用缺陷,随后研究表明大Panel可以替代全外显子测序来计算TMB,目前有越来越多的大panel出来,并且被证实这些几百个基因的panel可以达到与WES的高度相关性。然而,在之前的研究和临床研究中,TMB评估没有标准化。作为一种影响治疗决策的Biomarker,需要统一TMB评估方法,以获得可靠的、可比较的研究结果;另外,在实施TMB检测时,关键参数可能会影响工作流程、分析结果和数据解释。包括活检样本类型、样本质量和数量、基因组覆盖率、测序平台、生物信息学管线以及决定高TMB的最终阈值判断。
针对上述情况,在2019年10月15日,中国食品药品检定研究院就发布了关于TMB 注册检验用体外诊断试剂国家标准品和参考品说明书公示的通知,旨在告诉我们TMB检测性能评价需要合适的参考品,包括突变位点检测准确性评价,TMB检测一致性评价,和WES一致性评价,和具有临床药效样本检测一致性评价等。
而此次“肿瘤突变负荷检测国家参考品”的正式发布,有助于规范肿瘤突变负荷检测,推进肿瘤突变负荷检测的标准化和规范化。
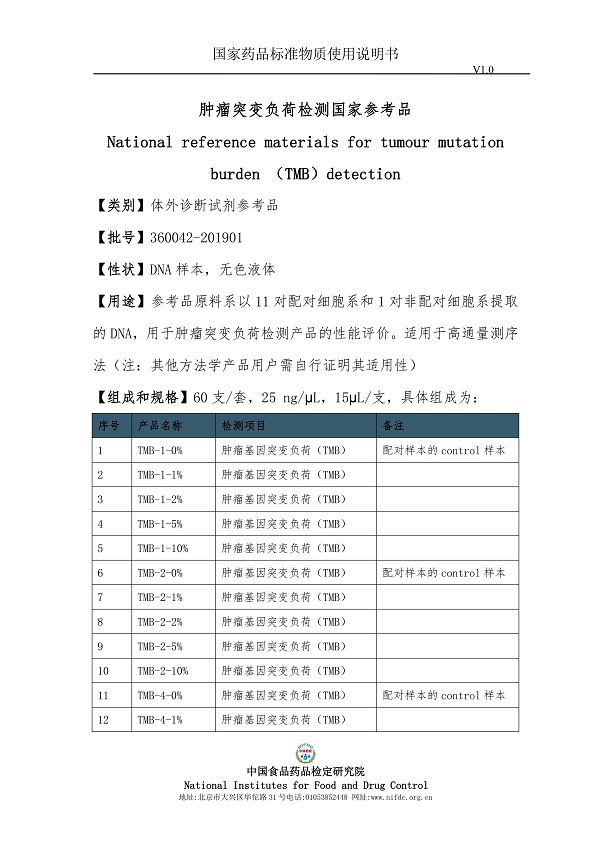
肿瘤突变负荷检测国家参考品包含11对配对细胞系和1对非配对细胞系提取的 DNA,用于肿瘤突变负荷检测产品的性能评价。适用于高通量测序法(注:其他方法学产品用户需自行证明其适用性)。该参考品共计60 支/套,25 ng/µL,15µL/支,其中的样品对均涵盖了0%,1%、2%、5% 和10%的肿瘤细胞系,分别提供了在1% 、2%、 3%、 4%、5% cutoff下的TMB值。


作为领先的标准品研发生产企业,菁良基因在标准品研发生产方面有着先进的技术和丰富的经验,在进行标准品研发设计和生产的过程中,充分调研了行业现状及问题,严格遵守相关法规及政策,积极为行业提供优质的产品和解决方案。菁良基因自成立起,就积极推进行业标准化及规范化的工作,以建立基因检测行业的金标准,提高基因检测的准确性,助力于患者的精准治疗为目标。
很荣幸此次菁良基因能够作为协作单位参与中检院肿瘤突变负荷检测国家参考品项目,未来,我们将继续秉持“质量第一、服务第一”的态度,在标准品领域不断研发、提升品质,确保持续稳定地提供更好的产品及服务。
相关链接
中国食品药品检定研究院《关于公布第八期注册检验用体外诊断试剂国家标准品和参考品目录的通知》
https://www.nifdc.org.cn/nifdc/twowebsite/twobzwz/twobzwztzgg/20200416160819529.html



